木质纤维素是地球上最丰富的可再生资源,其合成与降解是自然界碳素循环的中心环节。植物细胞壁在进化过程中形成了天然的“抗降解屏障”,特别是在半纤维素中,大多数多糖均含有侧链修饰,降解困难。青岛能源所微生物资源团队长期致力于嗜热微生物降解木质纤维素的机制研究,近期与美国北卡罗来纳州立大学的Robert Kelly教授合作,阐明了极端嗜热微生物Caldicellulosiruptor阿拉伯呋喃的酶解机制及其与木聚糖酶协同降解效应,对于木质纤维素的生物降解有重要意义,该成果发表在2017年的Applied Environmental Microbiology (AEM), 83:e00574-17上,微生物资源团队李福利研究员和吕明副研究员为该文通讯作者,同时申请发明专利一项。
此外,纤维素降解糖苷水解酶中,5家族为数众多,具有纤维素酶和地衣多糖酶等活性,但是双功能纤维素酶/地衣多糖酶底物的选择性机制尚不清楚。研究所微生物资源团队与代谢物组学团队冯银刚研究员、仿真模拟团队姚礼山研究员以及清华大学王新泉教授合作,解析了极端嗜热厌氧菌Caldicellulosiruptor sp. F32的糖苷水解酶F32EG5的蛋白及蛋白底物复合体结构,揭示了底物选择性机制。该工作已在线发表于Biochemical Journal上,李福利研究员和冯银刚研究员为该文的通讯作者。
研究团队发现F32EG5能够切断-1,3-1,4-葡聚糖底物的-1,3-糖苷键或 -1,3-糖苷键前面的 -1,4-糖苷键,与传统的GH16家族地衣聚糖酶(切断 -1,3-糖苷键后面的 -1,4-糖苷键)截然不同,是一种新的 -葡聚糖糖苷键切断方式。F32EG5具有典型的GH5家族蛋白( / )8桶状结构,具有独特的底物结合位点,决定了底物特异性。复合体结构显示,F32EG5具有一个急剧弯曲的底物结合孔道,与同样具有弯曲构象的 -1,3-1,4-葡聚糖底物特异结合,决定了该蛋白的高地衣聚糖酶活性。分子动力学模拟及定点突变分析验证了上述设想。
上述研究获得了科技部973计划、国家自然科学基金、山东省自然科学杰出青年基金、山东省重点研发计划等支持。(文/图 孟冬冬 吕明)
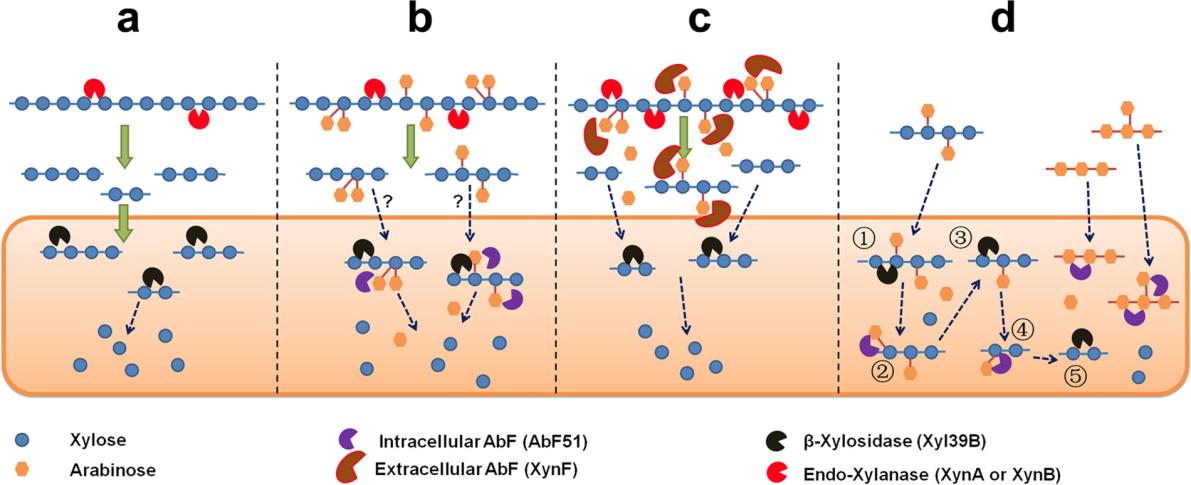
图1 Arabinofuranosidase协同降解带有阿拉伯糖侧链的半纤维素模式图
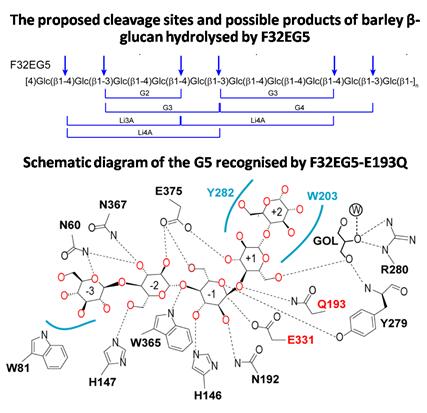
图2 F32EG5底物特异性作用机制
原文链接:
http://aem.asm.org/content/83/13/e00574-17.abstract?sid=d68d0570-f831-409f-83b8-df27cd7b2ea2
http://www.biochemj.org/content/early/2017/08/24/BCJ20170328